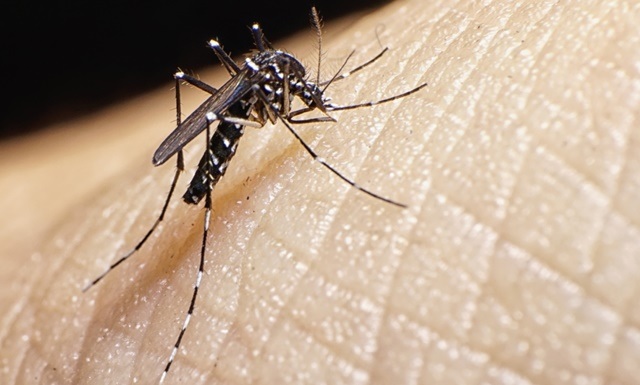
A Anvisa aprovou o pedido de registro definitivo da vacina contra chikungunya desenvolvida pelo Instituto Butantan em São Paulo, em parceria com a farmacêutica franco-austríaca Valneva. A decisão foi publicada no Diário Oficial da União nesta segunda-feira (14).
Com a aprovação, o imunizante está autorizado a ser aplicado no país na população acima de 18 anos. Esta é a primeira vacina autorizada contra a doença, que pode causar dor crônica nas articulações e afetou 620 mil pessoas no mundo só em 2024. Os países com mais casos da doença são Brasil, Paraguai, Argentina e Bolívia. O pedido de registro definitivo foi enviado à Anvisa em dezembro de 2023. No mesmo ano, a vacina foi aprovada pela agência regulatória norte-americana Food and Drug Administration (FDA).
No estudo clínico de fase 3, feito com adolescentes brasileiros após uma dose da vacina e publicado na “The Lancet Infectious Diseases” em setembro de 2024, foi observada a presença de anticorpos neutralizantes em 100% dos voluntários com infecção prévia e em 98,8% daqueles sem contato anterior com o vírus. A proteção foi mantida em 99,1% dos jovens após seis meses. A maioria dos eventos adversos registrados após a vacinação foi leve ou moderada, sendo os mais relatados dor de cabeça, dor no corpo, fadiga e febre.
Para que a vacina chegue aos braços da população, alguns passos ainda devem ser cumpridos. Segundo o governo de São Paulo, o Instituto Butantan ainda trabalha em uma nova versão, como parte do processo realizado no Brasil. As modificações usam componentes nacionais e serão mais adequadas à incorporação pelo Sistema Único de Saúde (SUS). A inclusão da vacina no Programa Nacional de Imunizações, no entanto, dependerá ainda de uma análise da Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec) e das demais autoridades de saúde.
Fonte: G1