Motivo de Faustão ter passado por transplante rapidamente mais uma vez

Quando passou por um transplante de coração, no ano passado, Faustão já sabia que os rins dele estavam comprometidos, tanto que estava passando por hemodiálise desde setembro. De acordo com familiares, a urgência foi pelo coração e, após se restabelecer, entraria na fila por um transplante de rim. Desde setembro, ele vinha fazendo sessões de hemodiálise, três vezes por semana, para retirar líquido do organismo. Em dezembro ele voltou à fila única do SUS por um novo rim. Mas o órgão deu sinais de piora devido a problemas de insuficiência cardíaca. Por isso a urgência de, mais uma vez, passar à frente na fila por um novo órgão. Na segunda-feira, 26, apresentador foi submetido ao transplante. Como funciona a lista do SUS Quando Faustão passou pela cirurgia no coração, o Ministério da Saúde explicou como funciona a lista de espera do SUS para transplantes, que é única, ou seja, vale tanto para os pacientes da rede pública quanto da rede privada. Quando um órgão fica disponível, é iniciada uma corrida contra o tempo para localizar o receptor compatível. No rol, além da gravidade do estado do receptor, são respeitados fatores como tipo sanguíneo, peso, altura e correspondência genética. “Todos os pacientes são regidos pelos mesmos critérios técnicos e entram na lista de acordo com as informações das equipes de transplante. De acordo com a gravidade, podemos movê-los dentro das listas”, disse Daniela Salomão, coordenadora-geral do Sistema Nacional de Transplantes, do Ministério da Saúde.
Lista das primeiras cidades do RJ que terão vacinação contra a dengue pelo SUS é revelada. Confira!
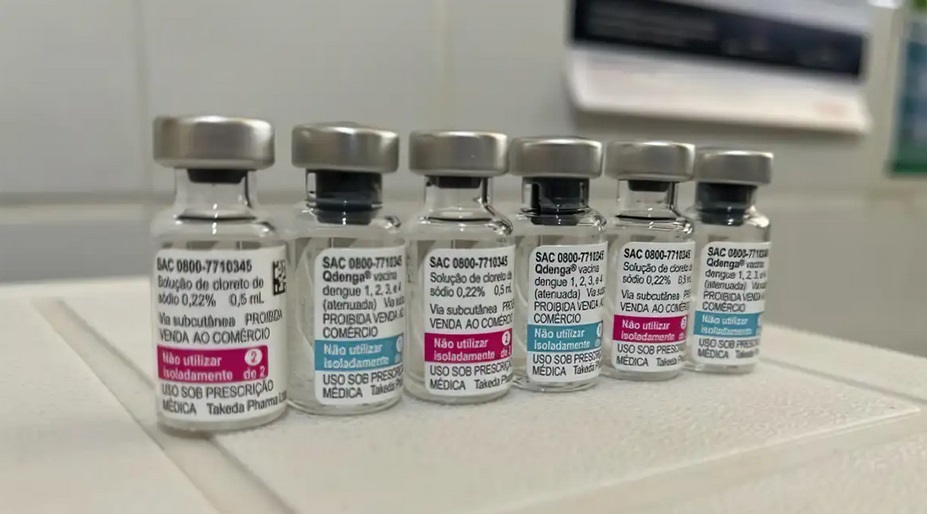
O Ministério da Saúde irá começar a aplicar a vacinação contra a dengue em fevereiro, quando 521 municípios brasileiros receberão as doses da vacina. No estado do Rio de Janeiro, as primeiras cidades a terem vacinação pelo SUS são a capital, Nilópolis, Duque de Caxias, Nova Iguaçu, São João de Meriti, Itaguaí, Magé, Belford Roxo, Mesquita, Seropédica, Queimados e Japeri. Em Campos, Macaé, São João da Barra, Cabo Frio e outras cidades do interior, não há previsão de quando começará a vacina. A lista completa dos municípios pode ser acessada aqui. As regiões selecionadas atendem a três critérios: são formadas por municípios de grande porte, com mais de 100 mil habitantes; registram alta transmissão de dengue no período 2023-2024; e têm maior predominância do sorotipo DENV-2. Conforme a lista, 16 estados e o Distrito Federal têm cidades que preenchem os requisitos. A pasta confirmou ainda que serão vacinadas crianças e adolescentes de 10 a 14 anos, faixa etária que concentra maior número de hospitalizações por dengue. Os números mostram que, de janeiro de 2019 a novembro de 2023, o grupo respondeu por 16,4 mil hospitalizações, atrás apenas dos idosos, grupo para o qual a vacina não foi autorizada. “A definição de um público-alvo e regiões prioritárias para a imunização foi necessária em razão da capacidade limitada de fornecimento de doses pelo laboratório fabricante da vacina. A primeira remessa com cerca de 757 mil doses chegou ao Brasil no último sábado. O lote faz parte de um total de 1,32 milhão de doses fornecidas pela farmacêutica.” “Outra remessa, com mais de 568 mil doses, está com entrega prevista para fevereiro. Além dessas, o Ministério da Saúde adquiriu o quantitativo total disponível pelo fabricante para 2024: 5,2 milhões de doses. De acordo com a empresa, a previsão é que sejam entregues ao longo do ano, até dezembro. Para 2025, a pasta já contratou 9 milhões de doses.” O esquema vacinal será composto por duas doses, com intervalo de três meses entre elas. O Brasil é o primeiro país do mundo a oferecer o imunizante no sistema público. A Qdenga, produzida pelo laboratório Takeda, foi incorporada ao SUS em dezembro do ano passado, após análise da Comissão Nacional de Incorporações de Tecnologias no SUS (Conitec).
Confira o que se sabe até agora sobre a vacina contra a dengue no SUS!

Há pouco mais de um mês, o Ministério da Saúde anunciou a incorporação da vacina contra a dengue no Sistema Único de Saúde (SUS). Antes disso, o imunizante Qdenga, produzido pelo laboratório japonês Takeda, passou pelo crivo da Comissão Nacional de Incorporações de Tecnologias (Conitec) no SUS, que recomendou a incorporação priorizando regiões do país com maior incidência e transmissão do vírus, além de faixas etárias de maior risco de agravamento da doença. A partir do parecer favorável da Conitec, o ministério reforçou que a vacina não seria utilizada em larga escala em um primeiro momento, já que o laboratório informou ter capacidade restrita de fornecimento de doses. A vacinação contra a dengue na rede pública, portanto, será focada em públicos específicos e em regiões consideradas prioritárias. “Até o início do ano, faremos a definição dos públicos-alvo levando em consideração a limitação da empresa Takeda do número de vacinas disponíveis. Faremos priorizações”, disse a ministra Nísia Trindade à época. O próximo passo seria um trabalho conjunto entre o Programa Nacional de Imunizações (PNI) e a Câmara Técnica de Assessoramento em Imunização (CTAI), programado para as primeiras semanas de janeiro, com o intuito de definir a melhor estratégia de utilização do quantitativo disponível da vacina. Segundo o laboratório Takeda, a previsão é que sejam entregues 5.082 milhões de doses entre fevereiro e novembro de 2024, sendo que o esquema vacinal da Qdenga é composto por duas doses, com intervalo de 90 dias entre elas. A avaliação de especialistas da CTAI é que o ministério deve seguir a recomendação da Organização Mundial da Saúde (OMS) e priorizar a vacinação contra a dengue na faixa etária entre 6 e 16 anos, conforme preconizou o Grupo Consultivo Estratégico de Peritos (SAGE, na sigla em inglês). A pasta, entretanto, informou que definiria, em conjunto com estados e municípios, qual a idade a ser priorizada dentro dessa janela, diante do quantitativo reduzido de doses. A vacina De acordo com a Sociedade Brasileira de Imunizações (SBim), a Qdenga é uma vacina tetravalente que protege, portanto, contra os quatro sorotipos do vírus da dengue – DENV-1, DENV-2, DENV-3 e DENV-4. Feita com vírus vivo atenuado, ela interage com o sistema imunológico no intuito de gerar resposta semelhante àquela produzida pela infecção natural. O imunizante deve ser administrado em esquema de duas doses, com intervalo de três meses entre elas, independentemente de o paciente ter tido ou não dengue previamente. Infecções prévias Quem já teve dengue, portanto, deve tomar a dose. Segundo a SBim, a recomendação, nesses casos, é especialmente indicada por conta da melhor resposta imune à vacina e também por ser uma população classificada como de maior risco para dengue grave. Para quem apresentou a infecção recentemente, a orientação é aguardar seis meses para receber o imunizante. Já quem for diagnosticado com a doença no intervalo entre as doses deve manter o esquema vacinal, desde que o prazo não seja inferior a 30 dias em relação ao início dos sintomas. Contraindicações Conforme especificado na bula, o imunizante é indicado para pessoas de 4 a 60 anos. Como toda vacina de vírus vivo, a Qdenga é contraindicada para gestantes e mulheres que estão amamentando, além de pessoas com imunodeficiências primárias ou adquiridas e indivíduos que tiveram reação de hipersensibilidade à dose anterior. Mulheres em idade fértil e que pretendem engravidar devem ser orientadas a usar métodos contraceptivos por um período de 30 dias após a vacinação. Eficácia Ainda de acordo com a SBim, a vacina demonstrou ser eficaz contra o DENV-1 em 69,8% dos casos; contra o DENV-2 em 95,1%; e contra o DENV-3 em 48,9%. Já a eficácia contra o DENV-4 não pôde ser avaliada à época devido ao número insuficiente de casos de dengue causados por esse sorotipo durante o estudo. Também houve eficácia contra hospitalizações por dengue confirmada laboratorialmente, com proteção geral de 84,1%, com estimativas semelhantes entre soropositivos (85,9%) e soronegativos (79,3%). Demais arboviroses A SBim destaca que a Qdenga é exclusiva para a proteção contra a dengue e não protege contra outros tipos de arboviroses, como zika, chikungunya e febre amarela. Vale lembrar que, para a febre amarela, no Brasil, estão disponíveis duas vacinas: uma produzida pela Fundação Oswaldo Cruz (Fiocruz), utilizada pela rede pública, e outra produzida pela Sanofi Pasteur, utilizada pelos serviços privados de imunização e, eventualmente, pela rede pública. As duas têm perfis de segurança e eficácia semelhantes, estimados em mais de 95% para maiores de 2 anos. Registro A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o registro da Qdenga em março de 2023. A concessão permite a comercialização do produto no país, desde que mantidas as condições aprovadas. O imunizante, contudo, segue sujeito ao monitoramento de eventos adversos, por meio de ações de farmacovigilância sob responsabilidade da própria empresa fabricante. Outros imunizantes A Qdenga é a primeira vacina contra a dengue aprovada no Brasil para um público mais amplo, já que o imunizante aprovado anteriormente, Dengvaxia, do laboratório francês Sanofi- Pasteur, só pode ser utilizado por quem já teve dengue. A Dengvaxia não foi incorporada ao SUS e é contraindicada para indivíduos que nunca tiveram contato com o vírus da dengue em razão de maior risco de desenvolver quadros graves da doença.
Estado do Rio terá política de fornecimento de canabidiol pelo SUS
O estado do Rio de Janeiro terá uma política estadual de fornecimento gratuito de medicamentos à base de canabidiol (CBD) e tetra-hidrocanabinol (THC) para pessoas que não têm condições financeiras de arcar com os custos desse tratamento. O acesso ao medicamento no estado será pelo Sistema Único de Saúde (SUS) e está previsto na lei 10.201/23, publicada nesta quarta-feira (6) no Diário Oficial. No Brasil, o tratamento com canabidiol foi liberado pela Anvisa para 12 tipos de doenças. A produção local, no entanto, não foi liberada para a população, o que faz com que o canabidiol usado no Brasil seja importado, encarecendo o medicamento e dificultando o acesso principalmente para pessoas de baixa renda. Pela nova lei estadual, para ter acesso aos medicamentos com canabidiol, o paciente deverá realizar o procedimento padrão do SUS, usando o Cartão Nacional da Saúde e seguindo as orientações atualizadas da Agência Nacional de Vigilância Sanitária (Anvisa). O paciente deverá apresentar a prescrição médica acompanhada de laudo, indicando que outros tratamentos foram testados e que o canabidiol é a melhor alternativa. Além disso, para obter o medicamento gratuitamente, deverá comprovar que não tem condições financeiras para ter acesso ao medicamento, seja ele importado ou vendido em farmácias brasileiras, e que a sua qualidade de vida depende desse tratamento. O paciente também deverá apresentar o Termo de Consentimento Livre e Esclarecido (TCLE) assinado em duas vias: uma para o médico e a outra para o paciente. O período de tratamento deverá ser indicado pela prescrição médica e pelo laudo. O tratamento deverá ser reavaliado a cada seis meses com o objetivo de verificar seus benefícios, bem como a necessidade de readequação, respeitando as especificidades do caso clínico do paciente. A coordenação das fases iniciais desse fornecimento deverá ser feita pela Farmácia Viva do SUS que, em convênio com as associações de pacientes, deverá acompanhar as etapas de coleta, processamento, armazenamento, preparação e dispensação dos produtos, para o acesso seguro e uso racional. A lei prevê ainda que o governo do estado desenvolva programas de investimento na formação técnico-científico e na capacitação de profissionais da área da saúde, farmacêutica e demais especialidades necessárias para a análise clínica, produção de pesquisas, criação de banco de dados, busca de novas tecnologias e inovação. O governo poderá, inclusive, criar um centro de estudo e tecnologia para promove políticas públicas de debate e fornecer informação a respeito do uso da CBD, de forma isolada ou associado ao THC. A lei também autoriza a criação de uma comissão de trabalho com a participação de técnicos do SUS, da Farmácia Viva e de representantes de associações de pacientes na produção de pesquisas científicas que orientem a atuação do SUS e garantam a segurança dos pacientes.

